
Estudio da pista sobre el síndrome inflamatorio multisistémico por COVID en niños
PorEFE
11/08/2021 - 3:29 pm
Artículos relacionados.
«Nuestro estudio ha descubierto que el agotamiento de las células T en los pacientes con SMI-C es uno de los posibles factores que impulsan esta enfermedad, lo que sugiere que un aumento tanto de las células NK como de las células T CD8+ agotadas en circulación podría mejorar los síntomas de la enfermedad inflamatoria», dijo Noam Beckmann.
Redacción Ciencia, 11 ago (EFE).- Un equipo de investigadores del Hospital Mount Sinai de Nueva York (EU) ha encontrado una pista importante sobre el origen del síndrome inflamatorio multisistémico o MIS-C (por sus siglas en inglés), una rara consecuencia asociada al coronavirus que afecta a algunos niños y que puede provocar la muerte.
La mayoría de los menores infectados con el SARS-CoV-2 pasan una enfermedad leve pero algunos desarrollan el MIS-C, una afección que inflama gravemente órganos y tejidos como el corazón, los pulmones, los riñones, el aparato digestivo, el cerebro, la piel o los ojos.
El MIS-C se considera un síndrome (un conjunto de signos y síntomas), no una enfermedad, porque hay muchas cuestiones que todavía se desconocen como la causa o los factores de riesgo.
La mayoría de los niños con este síndrome tienen entre tres y 12 años, y los más afectados tienen una edad promedio de ocho años.
Downregulation of exhausted cytotoxic T cells in gene expression networks of multisystem inflammatory syndrome in children | Nature Communications https://t.co/n6yM9rboSJ
— Matt Kennedy (@mekapk_kennedy) August 11, 2021
Sólo en Estados Unidos, desde que comenzó la pandemia, se han notificado 2 mil 600 casos.
Ahora, los investigadores del hospital de Nueva York han descubierto que determinadas células del sistema inmunitario que combaten la infección están poco activadas en los niños con MIS-C, y que esto se asocia a una respuesta inflamatoria sostenida, un sello distintivo del SARS-CoV-2.
El estudio, que se publica este miércoles en la revista Nature Communications, se hizo secuenciando el ARN de las muestras de sangre del Biobanco COVID-19 del Mount Sinai.
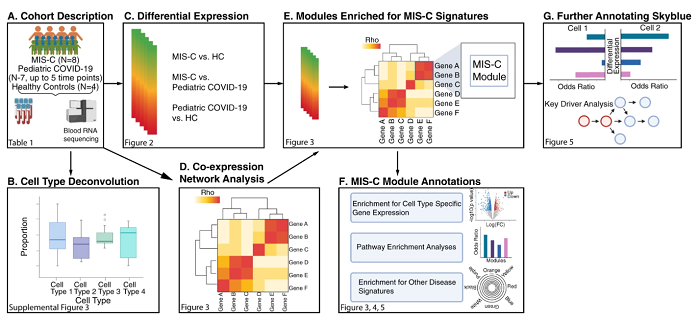
Gracias a un amplio estudio de expresión génica, los investigadores han dado un paso importante al proporcionar nuevas vías de exploración que implican complejas redes y subredes de genes analizadas en casos pediátricos de MIS-C y COVID-19 del Biobanco.
Una de las más significativas de estas redes de genes implicaba la supresión de dos tipos de células inmunitarias: las células asesinas naturales (NK) y las células T CD8+.
Investigaciones previas habían demostrado que cuando las células T CD8+ combaten de forma persistente a agentes patógenos, entran en un estado de «agotamiento» y pierden eficacia y capacidad de proliferación.
El nuevo estudio señala específicamente que en los casos de MIS-C, las células T CD8+ se encuentran en este estado de agotamiento, lo que podría debilitar la respuesta inmunitaria inflamatoria.
Además, el estudio también revela que el aumento de las células NK está asociado a las células T CD8+ agotadas.
«Nuestro estudio ha descubierto que el agotamiento de las células T en los pacientes con SMI-C es uno de los posibles factores que impulsan esta enfermedad, lo que sugiere que un aumento tanto de las células NK como de las células T CD8+ agotadas en circulación podría mejorar los síntomas de la enfermedad inflamatoria», explica Noam Beckmann, profesor en la Facultad de Medicina Icahn del Mount Sinaí.
El estudio, además, ha encontrado nueve reguladores clave de esta red de genes y apuntan que uno de ellos, el TBX21, es una prometedora diana terapéutica.
El Biobanco COVID-19 del hospital Mount Sinai es una iniciativa creada por un equipo de voluntarios formado por más de 100 enfermeras, médicos e investigadores, que sirve de base para toda la investigación sobre COVID-19 que se está desarrollando en el centro médico.