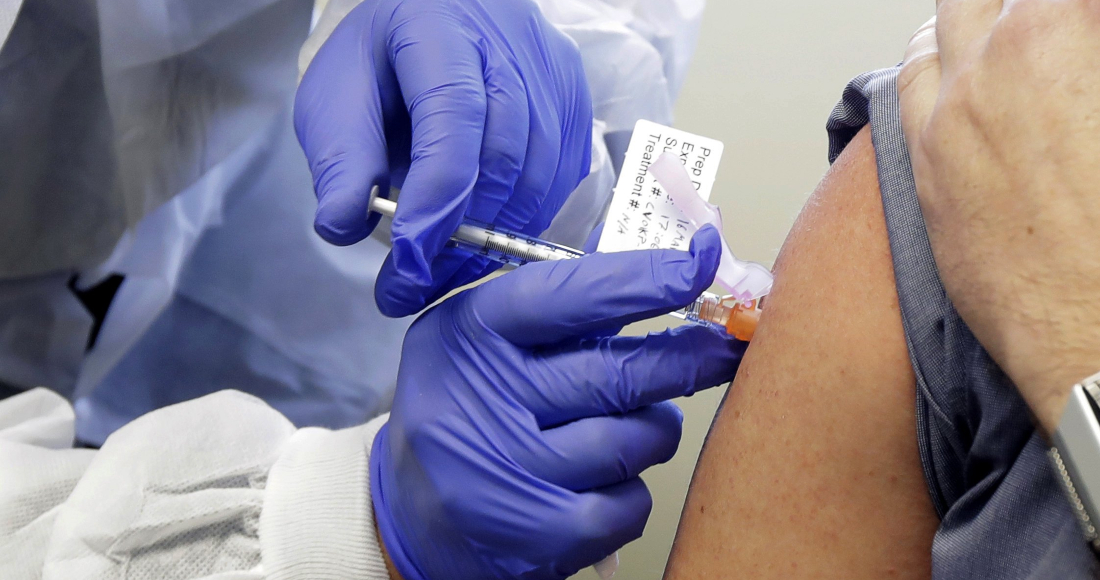
La Agencia Europea del Medicamento ha indicado que «las decisiones sobre la composición de la vacuna tendrán un impacto global», por lo que se discutirá una regulación armonizada.
Madrid, 3 de junio (Europa Press).- La Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha avanzado que las primeras vacunas contra la COVID-19 adaptadas a las nuevas variantes «podrían aprobarse en septiembre«.
En rueda de prensa este jueves, el organismo regulador europeo ha resaltado, no obstante, la necesidad de que estas nuevas vacunas sean iguales en todo el mundo.
«Las decisiones sobre la composición de la vacuna tendrán un impacto global», han detallado, recordando que las agencias de regulación de medicamentos a nivel mundial se reunirán el 30 de junio para discutir un «enfoque regulatorio armonizado».
[youtuebe ml0G44-poR8]
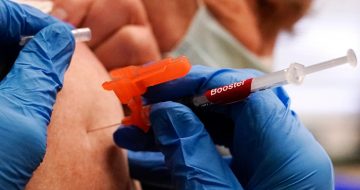
Mientras tanto, la EMA se encuentra evaluando el uso de la vacuna de Moderna en niños de 6 meses a cinco años, así como la dosis de refuerzo de Pfizer en niños de cinco a 11 años. También se están estudiando las solicitudes de autorización de comercialización presentadas por Valneva y Sanofi-Pasteur, así como la dosis de refuerzo de la vacuna de Novavax.
En cuanto a los tratamientos frente al coronavirus, la EMA ha precisado que, en el caso de la combinación de anticuerpos de AstraZeneca «Evusheld», «se podrían presentar datos para el tratamiento de la COVID-19 en pacientes con riesgo de desarrollar enfermedad grave». Este fármaco está actualmente indicado sólo para la prevención del coronavirus.