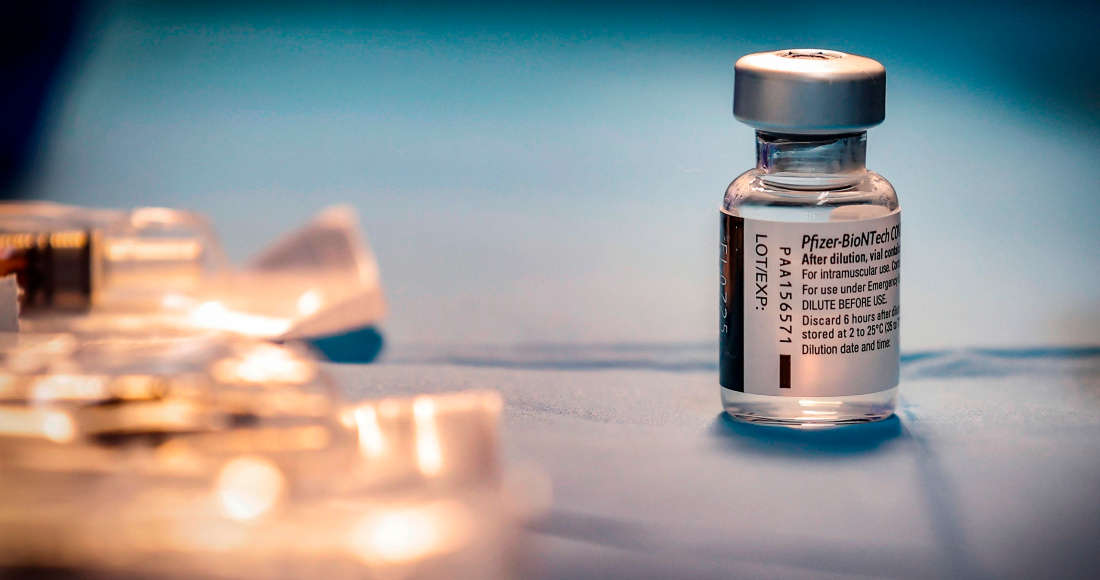
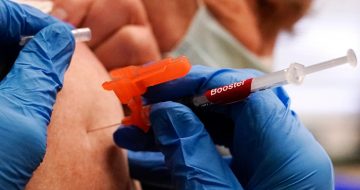
Para la empresa es "probable que se necesite una tercera dosis potenciadora entre seis y 12 meses después de la vacunación completa para mantener altos niveles de protección" contra el virus, y en especial contra Delta.
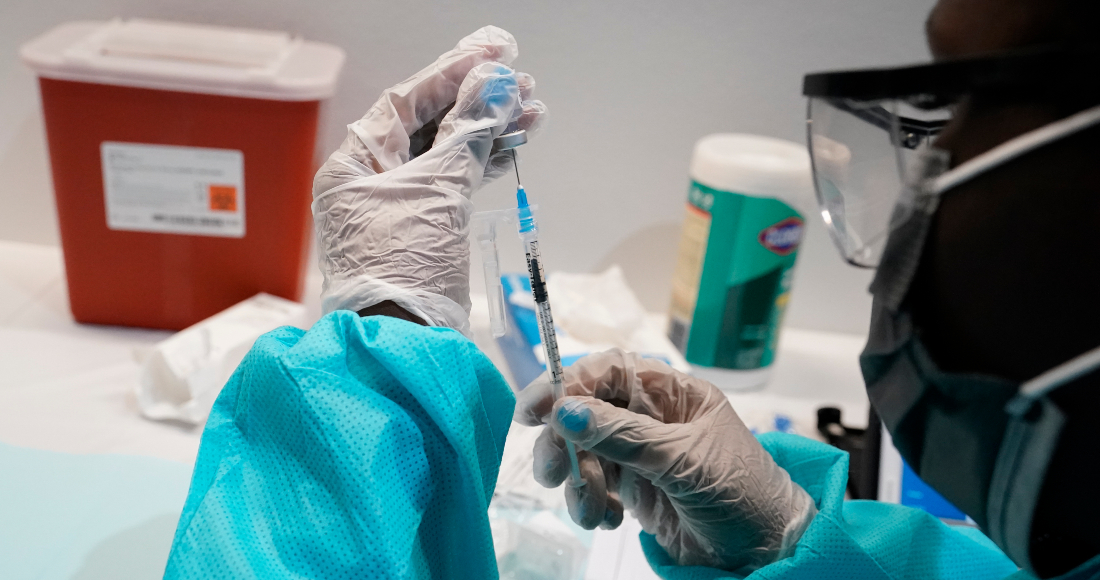
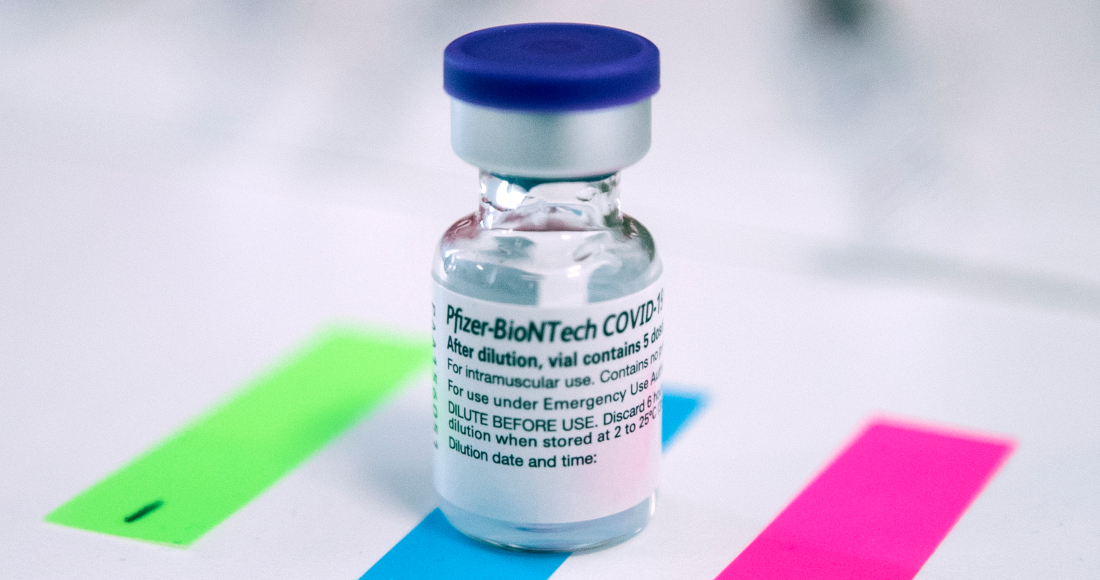
Nueva York, 28 jul (EFE).- La farmacéutica estadounidense Pfizer divulgó este miércoles que una tercera dosis de su vacuna contra la COVID-19 puede "impulsar con fuerza" la protección contra la variante Delta del coronavirus frente a una pauta de dos dosis, según datos preliminares de un estudio.
La empresa indicó en una presentación que sus datos sugieren que una tercera dosis produce niveles de anticuerpos contra la variante Delta cinco veces más altos en personas entre 18 y 55 años, y más de 11 veces en gente entre 65 y 85 años, en comparación con los niveles tras la segunda dosis.

Pfizer calcula que esa tercera dosis podría potencialmente multiplicar por 100 la neutralización de la variante Delta en comparación con una pauta de dos dosis, de acuerdo con el documento, que fue utilizado por la empresa en una conferencia telefónica para hablar de sus resultados financieros trimestrales.
Según explicaron ejecutivos en la conferencia, Pfizer cree "probable que se necesite una tercera dosis potenciadora entre seis y 12 meses después de la vacunación completa para mantener altos niveles de protección" frente a la COVID-19, y opinaron que la variante Delta es "la más transmisible" vista hasta ahora.
El estudio, que está en desarrollo y que no ha sido sometido a revisión de pares, parece indicar también que una tercera dosis suministrada al menos medio año después de la segunda es bien tolerada y genera niveles de anticuerpos altos contra el coronavirus original y la variante Beta.

Pfizer dijo a principios de este mes que pretendía solicitar una autorización a la Administración de Alimentos y Fármacos de EU (FDA, en inglés) para suministrar una tercera dosis de la vacuna anticovid, que ha desarrollado junto a la empresa alemana BioNTech.
"Las compañías esperan publicar datos más definitivos sobre el análisis y todos los datos acumulados serán compartidos como parte de las discusiones actuales con la FDA, la EMA (Agencia Europea del Medicamento) y otros reguladores en las próximas semanas", señaló la farmacéutica en una nota.