
¿Un corazón artificial, «puente al trasplante», para miles de pacientes? Sí, podría llegar al mercado este año
PorRedacción/SinEmbargo
31/01/2021 - 2:41 pm
Artículos relacionados.
- Gobiernos piden perdón por tragedia de 2011; Samuel García no va, deudos le reclaman
- La UdeG maneja millones al año. El poder de Padilla da más
- Cravioto acepta división de morenistas en el Senado: "No todos pensamos como Monreal"
- Creel presidirá la Mesa Directiva de la Cámara de Diputados; Mier dirigirá la Jucopo
- Balandra, la playa bonita de México, peligra por derrame
El dispositivo está diseñado para reemplazar un corazón natural durante unos cinco años para pacientes con insuficiencia cardíaca en etapa terminal.
Ciudad de México, 31 de enero (RT).- En diciembre del 2020, las autoridades médicas de Europa dieron el visto bueno para que Carmat, fabricante francés de corazones artificiales, pudiera comenzar a vender sus dispositivos, por ahora en forma de «puente al trasplante» y no de implante permanente, a partir del segundo trimestre de este año, recoge Reuters.
«Seguimos con nuestra ambición de tratar a todos los pacientes que necesitan un corazón», dijo a principios de mes el director ejecutivo de Carmat, Stephane Piat, además de señalar que la cantidad de posibles clientes es bastante grande. Según estimaciones, alrededor de 2 mil personas en Francia, Alemania, Italia, España y el Reino Unido están a la espera de un trasplante.
Contó que el dispositivo de Carmat, que se comercializará bajo la marca Aeson, estará disponible primero en Alemania, posiblemente seguida por Francia y otros países. Al mismo tiempo, declaró que uno de los principales desafíos para su empresa consiste en adquirir el reembolso por parte de los sistemas de seguridad social por el corazón artificial, cuyo precio por unidad superará los 150 mil euros (unos 182 mil dólares).
[youtube RCPBSO98kiY]
En su intento de expandirse en el mercado de trasplantes, Carmat anunció que este semestre comenzaría los estudios en EU con la esperanza de obtener la aprobación de parte de la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) para el año 2024.
FUNCIONAMIENTO
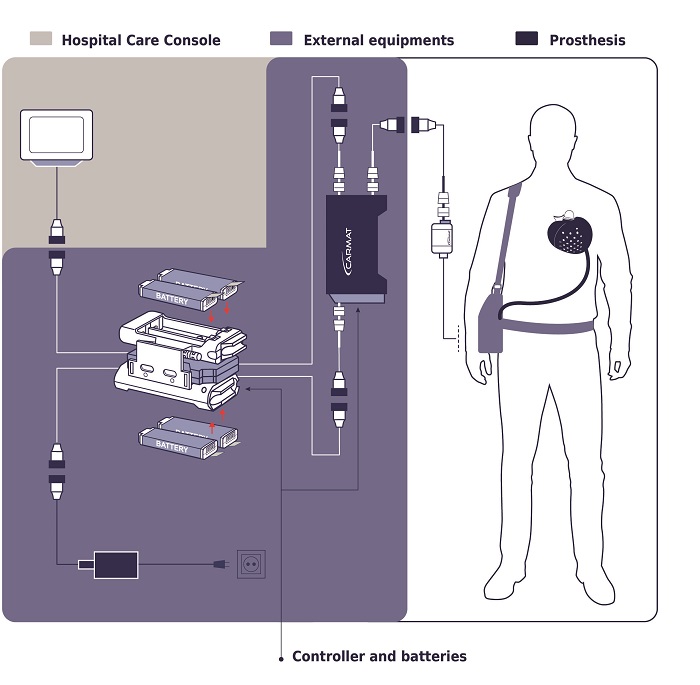
El mecanismo de Carmat está diseñado para reemplazar el corazón natural durante aproximadamente cinco años, imitando su trabajo con materiales y sensores biológicos. Su objetivo es prolongar la vida de miles de pacientes que mueren cada año mientras esperan un donante. Tiene un peso de 900 gramos, aproximadamente tres veces más que un corazón humano normal, y funciona con baterías de iones de litio.
Genera una circulación sanguínea de forma autónoma a nivel fisiológico. La prótesis está desarrollada a partir de los componentes, tanto orgánicos, como materiales utilizados en la industria aérea. Es por eso que además de médicos, participaron en su elaboración ingenieros de la empresa Matra Defense, del consorcio aeronáutico Airbus group.
HISTORIA
La aprobación de las autoridades regulatorias europeas concluyó un largo proceso de elaboración, que duró 27 años y también vio reveses.
En el 2008 Carmat presentó una revolucionaria prótesis como una solución a pacientes con insuficiencias cardíacas y que no tenían acceso a un donante natural. La compañía tardó varios años en obtener el permiso de las autoridades francesas para realizar cuatro estudios de viabilidad del procedimiento.
Sin embargo, la empresa se vio obligada temporalmente a suspender las pruebas clínicas de su corazón artificial, después de que el primer paciente falleciera dos meses y medio después de la intervención quirúrgica. Cabe señalar que antes de que le pusieran el dispositivo, el hombre había sufrido insuficiencia cardíaca terminal. Se estimaba que le quedaban sólo unas pocas semanas, o incluso días, de vida.
Carmat reanudó sus actividades en julio del 2014 y en septiembre de ese año llevó a cabo la segunda operación, esta vez con éxito. Para el 2016 Carmat logró operar a cuatro pacientes, y el programa fue extendido para incluir a dos grupos de 10 personas cada uno. En el 2018 la compañía aseguró que todos los participantes de uno de estos dos grupos mostraron «resultados positivos» en los ensayos clínicos.
En el 2017 Carmat envió a la Comisión Europea la solicitud para recibir la autorización para la distribución comercial de su producto, y al mismo tiempo continuó expandiendo los estudios.
Redacción/SinEmbargo
Sed ullamcorper orci vitae dolor imperdiet, sit amet bibendum libero interdum. Nullam lobortis dolor at lorem aliquet mollis. Nullam fringilla dictum augue, ut efficitur tellus mattis condimentum. Nulla sed semper ex. Nulla interdum ligula eu ligula condimentum lacinia. Cras libero urna,
https://dev.sinembargo.mx/author/redaccion/