Dos estudios han logrado crear en laboratorio estructuras parecidas a las de los embriones humanos. Sus hallazgos permitirán conocer más a fondo las primeras etapas del desarrollo humano y aportarán mayor conocimiento para los tratamientos de infertilidad.
Dublín, 17 mar (EFE).- Dos equipos de científicos han creado en el laboratorio «estructuras similares» a embriones tempranos a partir de células humanas, unos modelos que permitirán ampliar los conocimientos sobre las primeras etapas del desarrollo, la aparición de problemas congénitos al comienzo de la vida o nuevas terapias para tratar la infertilidad.
Ambos trabajos, presentados este miércoles en la revista Nature, abren ahora nuevas posibilidades en el campo de la embriología, ya que, hasta ahora, los investigadores han afrontado desafíos importantes.
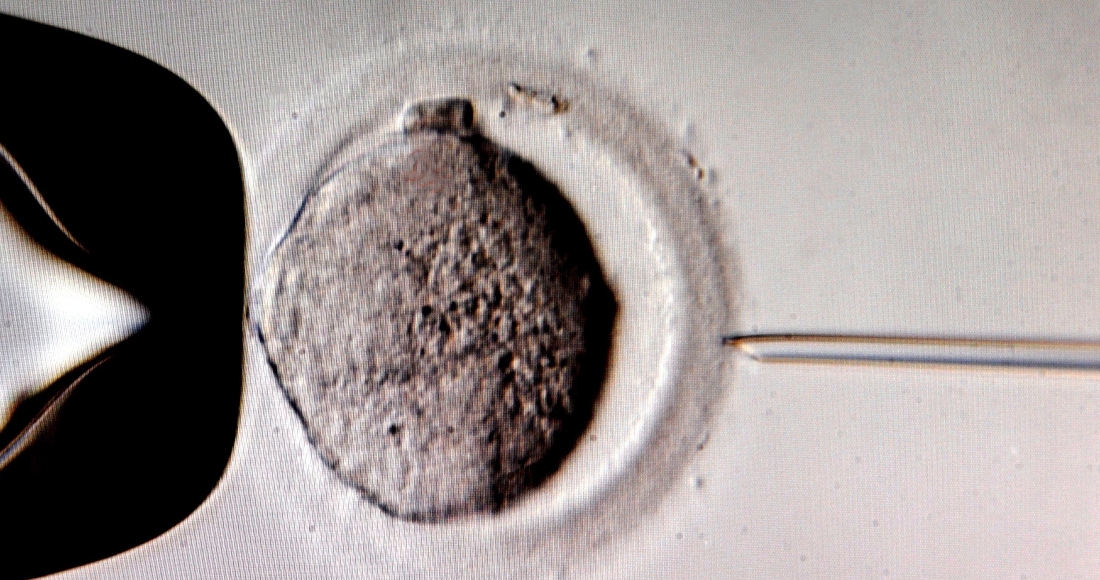
Recientemente, recordaron los autores en un encuentro virtual con los medios, se han generado, a partir de células de ratones, estructuras similares a los embriones de estos animales que se encuentran en la fase de blastocito -que ocurre unos cinco días después de su fertilización- y que se han llamado «blastoides».
Los blastocitos, explican, son estructuras esféricas formadas por una capa exterior de células que rodea a una cavidad líquida, en la cual se encuentra una masa de células embrionarias.
2/6 Congrats to the team led by @MonashBDI & @ARMI_Labs Prof Jose Polo, first authors Dr @ethanxdliu & PhD student Jia Ping Tan, with Dr @LabZenker, UWA’s Prof Ryan Lister, international collaborators A/Prof @OwenRackham & Prof @clarklabucla1. More: https://t.co/3K9NoPOi18 pic.twitter.com/cfGN8HBBsr
— Monash Biomedicine Discovery Institute (@MonashBDI) March 17, 2021
Los citados «blastoides» de ratones han permitido a los expertos replicar varios aspectos de su desarrollo temprano, pero presentan limitaciones para ahondar en el conocimiento sobre el inicio de la vida humana.
Aunque los blastocitos humanos obtenidos tras una fertilización in vitro han aportado a los investigadores, hasta la fecha, información valiosa, su disponibilidad y uso también son muy limitados, recuerdan.
Para superar estos obstáculos, el equipo liderado por el investigador argentino José Polo, de la Universidad Monash (Australia), ha generado, por primera vez, «blastoides» similares a los blastocitos con células humanas, lo que evitará así el uso de embriones naturales para llevar a cabo este tipo de estudios.
En concreto, reprogramaron fibroblastos, el principal tipo de célula del tejido conectivo, para producir modelos tridimensionales de blastocitos humanos, a los que han llamado «iBlastoides» («blastoides inducidos»).
Después constataron que los «iBlastoides» imitan la arquitectura general de los blastocitos y son capaces de dar lugar a células madre pluripotentes y trofoblásticas, un grupo de células que provee nutrientes al embrión y se desarrolla como parte importante de la placenta.
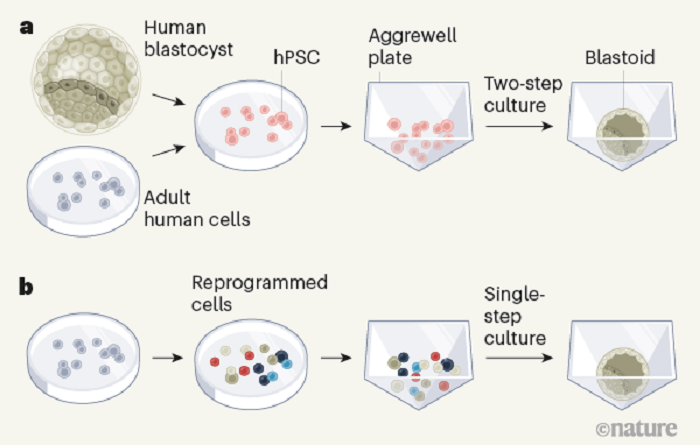
Aunque también lograron imitar varios aspectos de las primeras etapas de implantación, los autores advierten que los «iBlastoides» no deben considerarse como un «equivalente de blastocitos humanos».
5/6 Read the @nature publication titled: Modelling human blastocysts by reprogramming fibroblasts into iBlastoids. https://t.co/nA4CkSYeZN
— Monash Biomedicine Discovery Institute (@MonashBDI) March 17, 2021
ESTRATEGIA DE CULTIVOS
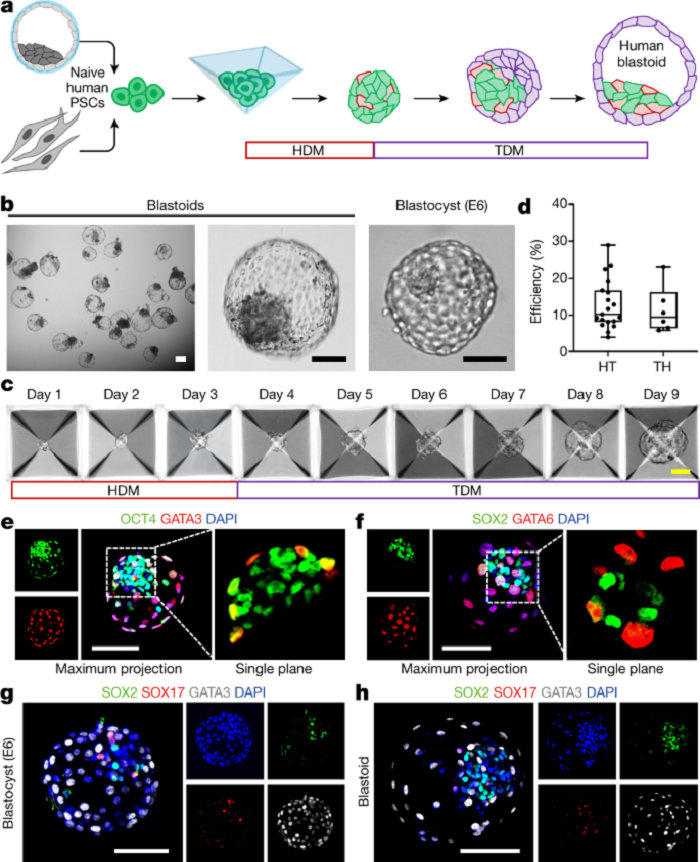
El segundo estudio, dirigido por Jun Wu, de la Universidad de Texas Southwestern (EU), presenta el desarrollo de una estrategia de cultivos tridimensional que permite generar estructuras similares a los blastocitos a partir de células madres pluripotentes, a las que han llamado «blastoides humanos».
Estos «conjuntos de células», expone Wu, se asemejan a los blastocitos humanos en su morfología, tamaño, número de células y en la composición de diferentes linajes de células.
Asimismo, los «blastoides humanos» son capaces de generar células madres embriónicas y extraembriónicas, al tiempo que pueden organizarse por sí mismos en estructuras con características propias de los embriones humanos periimplantarios.
Al igual que José Polo, Jun Wu subraya que estos «blastoides humanos» tampoco son «equivalentes» a los originales humanos, ya que, por ejemplo, no pueden dar vida a un embrión viable.
Los dos modelos descritos en Nature, celebran, llegan a reproducir «aspectos clave» del desarrollo temprano, pero presentan un número de diferencias respecto a los embriones humanos y, en consecuencia, no deben considerase como tales.
No obstante, dos expertos independientes, Yi Zheng y Jianping Fu, comentan en un artículo de análisis adjunto que, a medida que se optimizan los protocolos, estos blastoides llegarán a imitar con más precisión a los blastocitos humanos, lo que planteará cuestiones de carácter bioético.
Blastocyst-like structures generated from human pluripotent stem cells https://t.co/psJeMlezeo
— René Robles Cedeño (@reneroblesce) March 17, 2021
«En consecuencia -escriben-, el continuo desarrollo de modelos de embriones humanos, incluidos los blastoides humanos, demanda que se abran debates públicos sobre la importancia científica de estas investigaciones, así como sobre las cuestiones sociales y éticas que plantean».
Polo precisa que aún queda mucho para llegar a ese punto y que, de momento, están «entusiasmados» con el «gran número de aplicaciones» que ya ofrecen estos dos modelos de estudio para entender mejor «las funciones que tienen muchos genes en las primeras fases de desarrollo».
News & Views: Two Nature papers describe the generation of human blastocyst-like structures in the lab. The findings provide a model for studying early human development. https://t.co/YA3kGtFjHV
— Nature (@nature) March 17, 2021
«Además, estamos seguros de que nos llevará a comprender, por ejemplo, problemas de infertilidad y cómo resolverlos. O cómo, ya que podemos crear cientos de ellos (blastoides), pueden afectar toxinas y virus a esas primeras etapas», concluye.