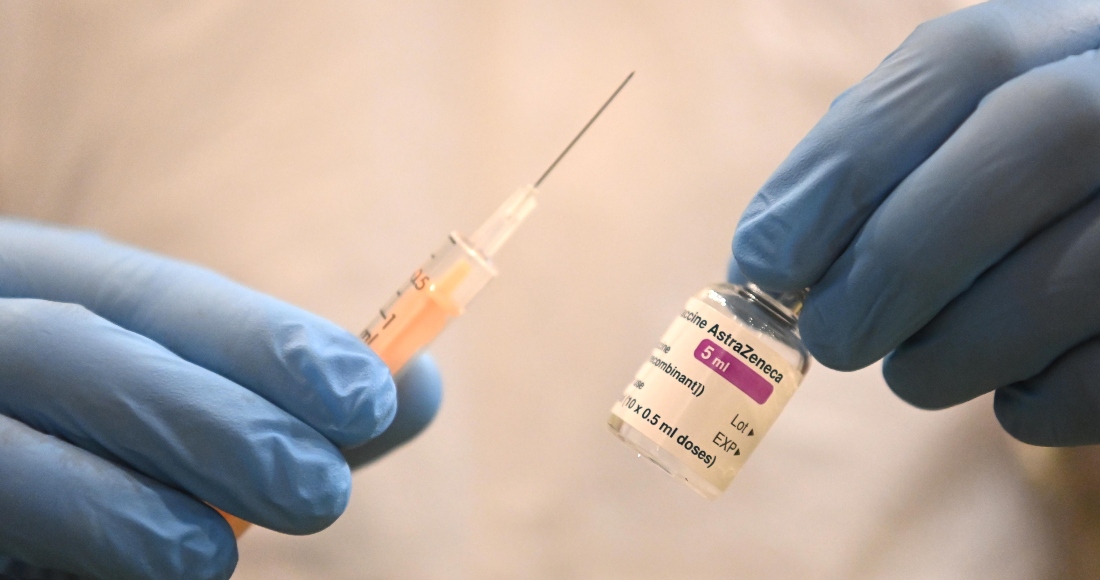
La Agencia Europea del Medicamento continúa su revisión de los casos de trombosis en personas vacunadas contra la COVID con AstraZeneca, aunque reiteró que, hasta el momento, no hay indicios de que la vacuna esté directamente relacionada con los eventos. De igual forma, anunció que el 18 de marzo dará a conocer las conclusiones de su investigación, así como las acciones que se deban en tomar, en caso necesario.
Bruselas, 15 mar (EFE).- El jefe de la unidad de amenazas biológicas a la salud y vacunas de la Agencia Europea del Medicamento (EMA), Marco Cavaleri, reiteró este lunes que este organismo sigue considerando que el beneficio de vacunarse con la fórmula de AstraZeneca sigue siendo superior a sus riesgos, tras detectarse varios casos de trombos en personas que recibieron este fármaco.
Cavaleri compareció ante la comisión de Salud Pública del Parlamento Europeo en una audiencia sobre las nuevas variantes del coronavirus y recibió preguntas sobre las garantías de seguridad en torno a esta vacuna, antes de que Italia, Francia y Alemania se unieran a la lista de países europeos que han suspendido su uso temporalmente.
«Estamos desarrollando una revisión rápida de toda la evidencia en torno a eventos tromboembólicos con esta vacuna para asegurar cuál es el beneficio y riesgo de su uso. No creemos que, hasta ahora, la evidencia que tenemos muestre un riesgo emergente afectando a sus beneficios. El beneficio-riesgo aún es considerado positivo y no vemos ningún problema en continuar la campaña de vacunación con ella», explicó Cavaleri en el Parlamento Europeo.

El científico de la EMA añadió que, en su proceso de revisión de la evidencia están «escrutando los datos» para intentar entender si este síntoma se da en grupos de personas que compartan alguna patología, antecedente o problema médico específico, con vistas a «refinar» los grupos a los que se les administra este fármaco en concreto.
La EMA recordó que la pandemia es “una crisis mundial, con un impacto sanitario, social y económico devastador”, y las vacunas “ayudan a proteger a las personas”.
EMA’s safety committee (#PRAC) continues investigation of the #COVID19vaccine Astra Zeneca and thromboembolic events. Check out the latest updates:
?https://t.co/5u3ltzNuYd— EU Medicines Agency (@EMA_News) March 15, 2021
Distintos países europeos han identificado casos de trombosis entre los vacunados con esta formula e investigan si hay una relación de causa y efecto, aunque la EMA ya recomendó el pasado jueves «seguir administrando» la vacuna contra la COVID-19 de AstraZeneca en la Unión Europea (UE).

El comité de seguridad (PRAC) de la EMA concluyó que, de momento, «no hay indicios de que la vacunación haya causado estas afecciones, que no se enumeran como efectos secundarios de esta vacuna».
El comité ha analizado durante el fin de semana, y seguirá durante los próximos días, «todos los datos relacionados con eventos tromboembólicos» y ha convocado una reunión extraordinaria el jueves 18 de marzo para anunciar sus conclusiones «y cualquier otra acción que pueda ser necesaria» con relación a la vacuna de AstraZeneca.
«El número de eventos tromboembólicos en personas vacunadas no es mayor que el número observado en la población general», asegura la EMA, que recibió hasta este jueves la notificación de 30 casos de episodios similares entre cerca de cinco millones de personas inmunizadas con el fármaco de AstraZeneca en la UE.
El PRAC sigue investigando los casos reportados en días posteriores a la inyección con AstraZeneca, cuyos efectos secundarios más comunes suelen ser «leves o moderados, y mejoran unos días tras la vacunación».
Oficialmente no se encuentran entre ellos posibles eventos tromboembólicos, puesto que no fueron detectados en los ensayos clínicos llevados a cabo antes de lograr su licencia en la UE.
Alemania, España, Francia, Italia, Dinamarca, Noruega, Islandia, Bulgaria, Irlanda y Países Bajos han suspendido el uso de la vacuna, mientras que varios como Austria, Estonia, Letonia, Lituania y Luxemburgo retiraron un lote en concreto al detectar casos de trombosis.

La EMA considera la decisión de estos países como una “precaución tomada a la luz de su situación nacional”, pero subrayó que los eventos que “involucran coágulos de sangre, algunos con características inusuales como un bajo número de plaquetas, han ocurrido en un número muy pequeño de personas que recibieron la vacuna”.
Además, recordó que “miles de personas desarrollan coágulos de sangre anualmente en la Unión Europea por diferentes razones y el número de eventos tromboembólicos en general en las personas vacunadas no parece ser mayor que el observado en la población general”, una situación que podría suponer que los casos detectados en vacunados sean una coincidencia, y no un caso de efecto secundario del fármaco de AstraZeneca.
“Los expertos están analizando con gran detalle todos los datos disponibles y las circunstancias clínicas que rodean casos específicos para determinar si la vacuna pudo haber contribuido o si es probable que el evento se deba a otras causas”, añade la EMA, que informa de que el PRAC revisará más a fondo la información en una reunión prevista para mañana.
La agencia recomienda comunicarse con las autoridades sanitarias a las personas que “sospechan que pueden tener un efecto secundario después de la vacunación”, mientras sus expertos estudian la situación junto con la farmacéutica AstraZeneca, especialistas en trastornos sanguíneos y otras autoridades sanitarias, incluida la agencia británica reguladora de medicamentos (MHRA).
NO HAY PRUEBAS DE QUE LA VACUNA PRODUZCA COÁGULOS: MHRA
La agencia británica reguladora del medicamento (MHRA, en inglés) señaló este lunes que las pruebas existentes no apuntan a que la vacuna de AstraZeneca cause coágulos sanguíneos en sus receptores, algo que también defendió la farmacéutica en un comunicado.
«Estamos examinando de cerca los informes, pero teniendo en cuenta el gran número de dosis administradas y la frecuencia con que pueden ocurrir los coágulos sanguíneos de forma natural, las pruebas disponibles no indican que la vacuna sea la causa», destacó el responsable de seguridad de las vacunas en la MHRA, Phil Bryan.
People should still go and get their vaccine when asked to do so.
Read our response to Irish authorities’ action to temporarily suspend the AstraZeneca #COVID19 Vaccine: https://t.co/uV1msKuEfO pic.twitter.com/07XY2hXfjY
— MHRAgovuk (@MHRAgovuk) March 14, 2021
El regulador salió así al paso de la decisión de Irlanda, anunciada el domingo, de suspender temporalmente la aplicación del preparado de AstraZeneca contra la COVID-19.
«La gente debería seguir yendo a ponerse su vacuna contra la COVID-19 cuando se les pida», agregó Bryan en un comunicado.
La intervención del regulador británico se produce después de que la propia compañía farmacéutica emitiese anoche un comunicado en el que reiteraba la seguridad de su producto y negaba que produjese coágulos.

«Una cuidadosa revisión de todos los datos disponibles de más de 17 millones de personas vacunadas en la Unión Europea y el Reino Unido con la vacuna de AstraZeneca contra la COVID-19 no ha mostrado ninguna prueba de un mayor riesgo de embolia pulmonar, de trombosis venosa profunda (TVP) o de trombocitopenia en ningún grupo de edad, género, lote o en un país particular», dijo.
Según los datos recopilados por la compañía, hasta el 8 de marzo ha habido 15 casos de TVP y 22 de embolias pulmonares entre los receptores de la vacuna en la UE y el Reino Unido.
Esa proporción, subraya AstraZeneca, «es mucho más baja de lo que podría esperarse de forma natural en una población general de ese tamaño, y es similar a la de otras vacunas con licencia contra la COVID».
Además, insiste, el número de trombos producidos entre quienes participaron en los ensayos clínicos, pese a ser bajo, fue todavía menor en quienes recibieron la vacuna y no un placebo.
Tampoco hubo, subraya la compañía anglo-sueca, pruebas de un mayor sangrado entre los 60 mil participantes en los ensayos.
«En cuanto a la calidad, tampoco se ha confirmado ningún problema relacionado con algún lote de nuestra vacuna usado en Europa o el resto del mundo. Se han hecho y se están haciendo test por nuestra parte y de forma independiente por las autoridades sanitarias europeas y ninguno de estos muestra causas para preocuparse», reitera.

La semana que viene la Agencia Europea del Medicamento (EMA, en inglés) publicará su informe mensual de seguridad en su página web, recuerda AstraZeneca.