Brasil espera en el primer semestre, con una combinación propia de vacunas importadas y otras producidas en el país del inmunizante de AstraZeneca, tener 110 millones de dosis, equivalentes a la mitad de la población y para lo cual el Gobierno federal ya reservó los recursos en su presupuesto estatal.
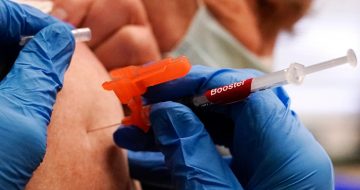
Recife (Brasil), 3 de enero (EFE).- La Agencia Nacional de Vigilancia Sanitaria (Anvisa) de Brasil autorizó la «importación excepcional» de dos millones de dosis de la vacuna contra la COVID-19 producida por el laboratorio anglo-sueco AstraZeneca y la universidad británica de Oxford, según informó este domingo el órgano regulador.
El pedido, según un comunicado de la Anvisa, fue realizado por el laboratorio estatal Fiocruz, que será el encargado de la administración de las dosis importadas y de la producción local a partir del acuerdo de transferencia de tecnología establecido entre el consorcio británico y el Gobierno brasileño.
No obstante, aclaró el ente regulador, las dosis que deberán llegar al país este mes no podrán ser suministradas todavía a las personas porque «el inmunizante no fue sometido a la autorización de uso en carácter de emergencia o de registro sanitario de definitivo».
«La importación excepcional es una preparación para anticipar la disponibilidad de vacunas a partir de que el producto sea aprobado por la agencia», completó el organismo.
Brasil espera en el primer semestre, con una combinación propia de vacunas importadas y otras producidas en el país del inmunizante de AstraZeneca, tener 110 millones de dosis, equivalentes a la mitad de la población y para lo cual el Gobierno federal ya reservó los recursos en su presupuesto estatal.
Las dosis que llegarán este mes, apuntó la Anvisa, fueron producidas en la India por el Serum Institute y forman parte de la plataforma Covaxx Facility, un programa global de la Organización Mundial de la Salud (OMS) para garantizar antivirus a todos los países y del cual Brasil forma parte.
Fiocruz, de acuerdo con las normas de la Anvisa, deberá responder por el almacenamiento adecuado y seguridad de las dosis, como ocurrió ya con la importación de las vacunas del laboratorio chino Sinovac, que tiene un acuerdo de transferencia de tecnología con el estatal Instituto Butantán, de Sao Paulo.
En total, el estado de Sao Pulo ya recibió 10.6 millones de dosis y deberá presentar a la Anvisa el resultado de la tercera fase de estudios y el nivel de eficacia el próximo 7 de enero, mientras que la documentación de AstraZeneca espera ser entregada una semana después, el día 15.
Además de las vacunas china y británica, la del consorcio estadounidense-alemán Pfizer-BioNTech y la de la belga Janssen, brazo europeo de la multinacional norteamericana Johnson & Johnson, realizan en Brasil estudios de tres fases con voluntarios que han recibido las dosis.
Sin embargo, ninguno de los fabricantes han pedido el aval para el uso en carácter de emergencia del inmunizante ni terminado de presentar los documentos necesarios para la autorización de la aplicación de las vacunas.
La vacuna rusa «Sputnik V», por no tener estudios realizados en el país con voluntarios, no forma parte del cuadro actual de inmunizantes considerado por la Anvisa, pero podrá ser incluida con la «conclusión de un análisis de pedido», según subrayó el regulador brasileño.